
Вещество, которое поможет защитить лёгкие

Российские учёные из Уральского федерального университета разработали новый вид химических соединений, способных подавлять тяжёлое воспаление в лёгких, при этом не угнетая иммунитет. Результаты исследования опубликованы в журнале Pharmaceuticals.
– Сейчас используется дексаметазон, гормональный препарат, но это вещество угнетает иммунитет. В составе нового вещества – азолоазиновые гетероциклы. Они способны подавлять активность интерлейкина-6 (группа молекул, которая играет большую роль в иммунном ответе, но при этом может вызывать неконтролируемое воспаление, разрушение тканей). Новые соединения демонстрируют такой же противовоспалительный эффект, как при дексаметазоне, но при этом помогают удерживать эту опасную реакцию. Благодаря разработке на фармацевтическом рынке могут появиться новые лекарственные средства для лечения тяжёлых форм гриппа и COVID-19, – рассказывает Анна Маринович, руководитель отдела научных коммуникаций Уральского федерального университета.
Метод контроля доставки "лечебных генов" в клетки
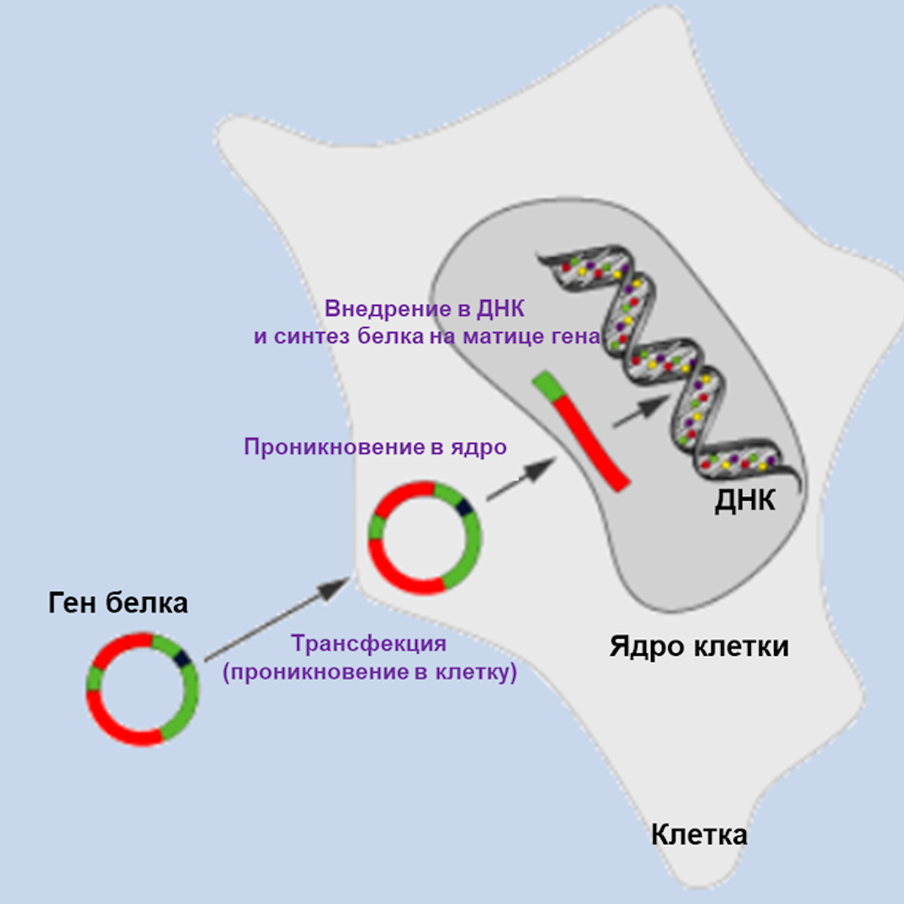
Российские учёные из Научно-исследовательского института биомедицинской химии имени В. Н. Ореховича (ИБМХ) разработали новый метод электрохимической регистрации процесса ДНК-трансфекции, позволяющий наиболее эффективно оценивать надёжность доставки генов в живые клетки с целью лечения болезней. Результаты работы опубликованы в международном научном журнале Journal of Electroanalytical Chemistry.
– Процесс внедрения материала в клетку называется трансфекцией, – рассказывает Дмитрий Жданов, доктор биологических наук, заведующий лабораторией медицинской биотехнологии НИИ им В. Н. Ореховича. – Эта процедура – мощный инструмент, помогающий не только изучать клеточные процессы и молекулярные механизмы заболеваний, но и проводить коррекцию генетических нарушений. Раньше в процессе трансфекции мы использовали так называемый репортёрный ген. Он кодирует светящийся белок. То есть белок, который мы доставляли в клетки, окрашивали в зелёный цвет – и таким образом могли его отследить. Клетки, которые светятся, подверглись трансфекции, ген в них доставлен. В них произошло изменение. Зелёный белок тяжёлый, много весит. Чем тяжелее генетический материал, тем труднее он проходит в клетку. В новом методе мы предлагаем отказаться от зелёного белка. Это уменьшит размер генетического материала и увеличит эффективность трансфекции. Количество трансфицированных клеток будет больше. Вероятность успеха повышается.
Титановые нанопокрытия

Российские учёные из Томского политехнического университета вместе с коллегами из разных стран разработали покрытия на основе оксидов и оксинитридов титана, которые продлят срок службы коронарных стентов, помогут защитить их от холестериновых бляшек и уменьшат риск тромбообразования. Предложенный метод создания покрытий также будет востребован в полупроводниковой промышленности и оптике. Результаты опубликованы в журнале Journal of Colloid and Interface Science.
– Сердечно-сосудистые заболевания находятся на одном из первых мест по смертности, – рассказывает Сергей Твердохлёбов, и. о. руководителя лаборатории плазменных гибридных систем ТПУ. – И самая большая проблема – когда сосуды зарастают холестериновыми бляшками. К счастью, это научились лечить: вставляют внутрь сосуда специальную трубочку, раздувают миниатюрным баллоном, и сосуд расширяется. Но это может дать краткосрочный эффект, так как бляшки могут вновь на сосуде образоваться. Тогда эту часть сосуда приходится вырезать и заменять другим сосудом. Во всём мире борются за то, чтобы эффективность кардиологического стента была высокой. Совместно с нашими коллегами из ТПУ и НИИ кардиологии Томского национального исследовательского медицинского центра РАН мы предложили комбинированное решение: наносить оксинитридное покрытие и поверх него специальный биорезорбируемый композит с наночастицами. Исследования покрытий на основе оксинитридов титана показали биологическую эффективность азотсодержащих покрытий.
Молекулярная основа новых обезболивающих лекарств
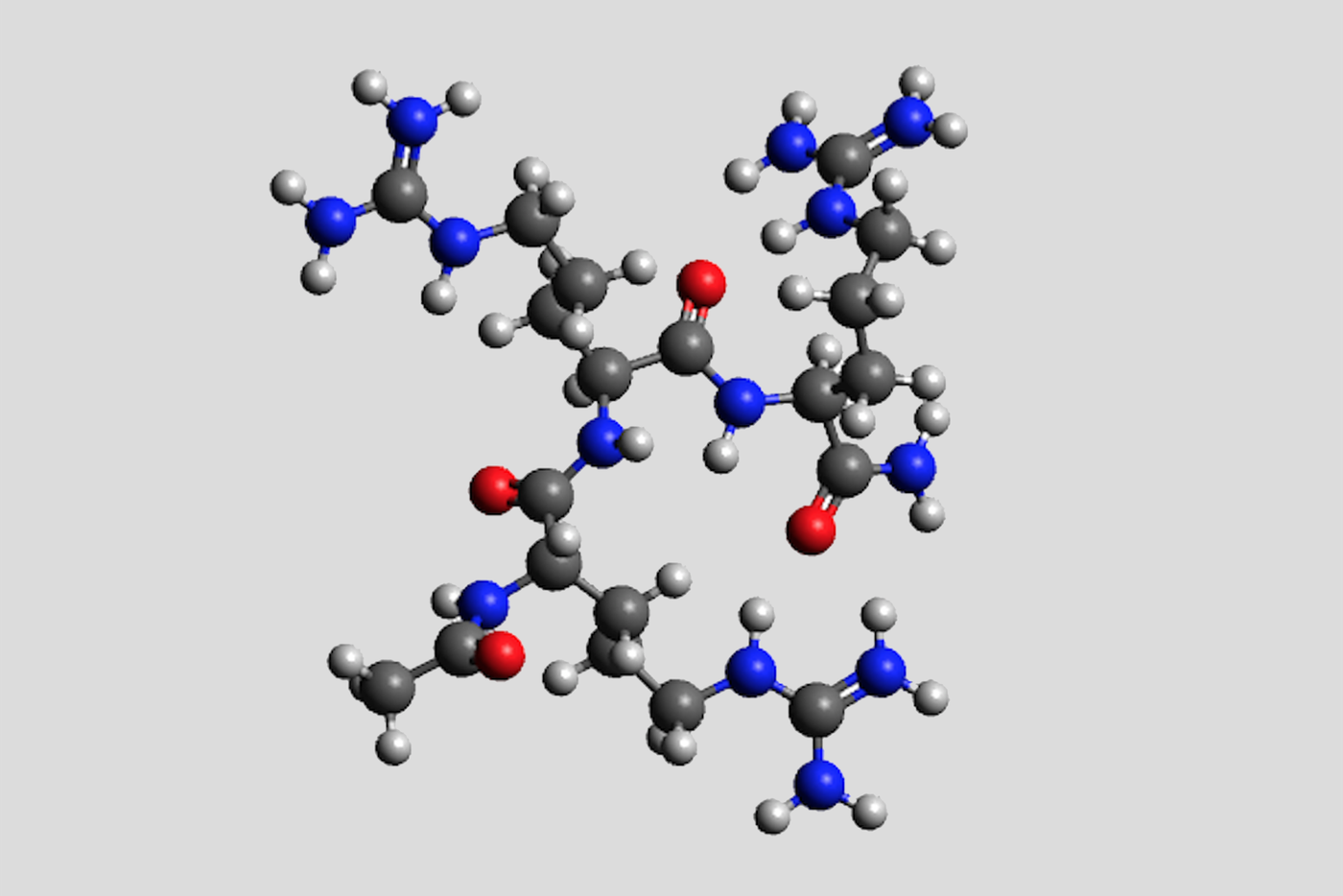
Российские учёные из Института физиологии имени И. П. Павлова и Физико-технического института имени А. Ф. Иоффе РАН нашли молекулы, которые могут быть основой новых обезболивающих лекарств, не вызывающих привыкания. Результаты работы опубликованы в международном журнале International Journal of Molecular Sciences.
– На сегодня в арсенале практической медицины отсутствуют безопасные и эффективные анальгетики, хотя спрос на них огромен: сотни миллионов людей во всём мире страдают от хронической боли, – рассказывает Борис Крылов, доктор биологических наук, заведующий лабораторией физиологии возбудимых мембран Института физиологии. – Пациентам с острой болью, онкологической болью, а также с различными видами хронической боли качество жизни можно повысить в ряде случаев только назначением препаратов из группы опиатов. Их длительное применение вызывает привыкание и приводит к необратимым негативным побочным эффектам. Мы исследуем на молекулярном уровне, как возникает болевой сигнал (он же, по сути, является электрическим импульсом), как можно управлять его характеристиками, чтобы ослабить или полностью купировать болевой синдром. Нам удалось обнаружить короткую пептидную молекулу, состоящую из трёх одинаковых остатков натуральной аминокислоты – аргинина. Она способна связываться с молекулой так называемого медленного натриевого канала. Медленные натриевые каналы – это весьма большие белки, находящиеся в мембранах нервных клеток. Они участвуют в кодировании болевого сигнала в нервной системе. Выяснилось, что синтезированная по нашему дизайну пептидная молекула может снижать функциональную активность медленных натриевых каналов таким образом, что болевой ответ "выключается", а информация о других ощущениях продолжает передаваться мозгу. Это делает перспективным создание на её основе нового анальгетического лекарственного средства.